名词解释:
FIC(first in class):指基于最新疾病学研究找到一些候选靶点,从0到1合成候选化合物,通过反复试验筛选,最终发现满足治疗效果与人体安全性要求的药物。FIC药物是相同作用机制药品中首个上市的药品,或者在研药品中进度处于全球领先/同步的药品。
ME-TOO/ME-BETTER/BIC(best in class)类药物:指根据公开的FIC药物信息,在其原有结构上进行合理修改,得到一个分子结构和FIC药物不同,而药效近似的药物。根据实际疗效的优劣程度,依次分为BIC、ME-BETTER、ME-TOO等多种类型。
特异性(细胞免疫概念):是指通过体外培养患者自身的抗癌细胞,患者体内缺少什么细胞,培养什么细胞,然后回输到患者体内,达到科学抗癌的目的。
浓度梯度动态平衡:通常发生在细胞边界或膜的两侧。如果粒子可以自由穿过膜即扩散的过程,则粒子由高浓度向低浓度区域净流动,最终导致两个区域的浓度变得相等,这种状态被称为动态平衡。
靶向治疗:又称“生物导弹”,是在细胞分子水平上,针对已明确的致癌位点的治疗方式,该药物在体内特异地选择致癌位点,结合并作用与肿瘤细胞的特异性死亡,不会波及肿瘤周围的正常组织细胞。
(一)基本定义
创新药,是一个相对于“原研药”和“仿制药”的概念,境内外均未上市,具有明显临床应用价值和优势的新药创新药。创新药强调新颖的化学结构或新的治疗用途,具备完整充分的安全性有效性数据作为上市依据,首次获准上市且具有自主知识产权的药物。它是在已有药物的基础上做一些改进,比如通过结构修饰,使药物的生物利用率更高。
(二)主要分类
国际惯例一般将创新药分为了首创新药和仿制创新药两类,其中首创新药主要指的是FIC(first in class)药物,而仿制创新药也叫“派生药”,包括me-too /me-better/best in class等数种药物。
(1)按注册类别分类。2020年7月,国家药监局出台了新版化药&生物制品注册分类,其中化学药注册分类主要包括5类。治疗用生物制品包含3类。根据政策规定以及当前国内创新药行业发展现状,可将1类、2类化学药和治疗用生物制品归为创新药。

表1 我国创新药注册分类
(2)根据原料来源、生产工艺等分类。我国创新药一般可以分为化学小分子创新药和生物大分子创新药。
化学小分子创新药:指化学合成药物,通常分子量小于1000的有机化合物。作为是信号传导抑制剂,它能够特异性地阻断肿瘤生长、增殖过程中所必需的信号传导通路,从而达到治疗的目的。
生物大分子创新药:也被称为生物制品(包括多肽、融合蛋白、重组血浆因子、抗体、聚糖与核酸等),是指以基因工程、细胞工程、蛋白质工程、发酵工程等生物技术获得的微生物、细胞及各种动物和人源组织和液体等生物材料制备的药品。多用于预防、治疗和诊断肿瘤、艾滋病、心脑血管病、肝炎等重大疾病。
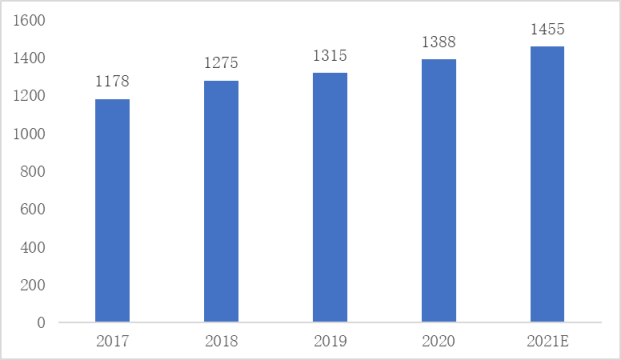
表2 化学小分子创新药与生物大分子创新药的区别
二、我国创新药行业宏观政策分析
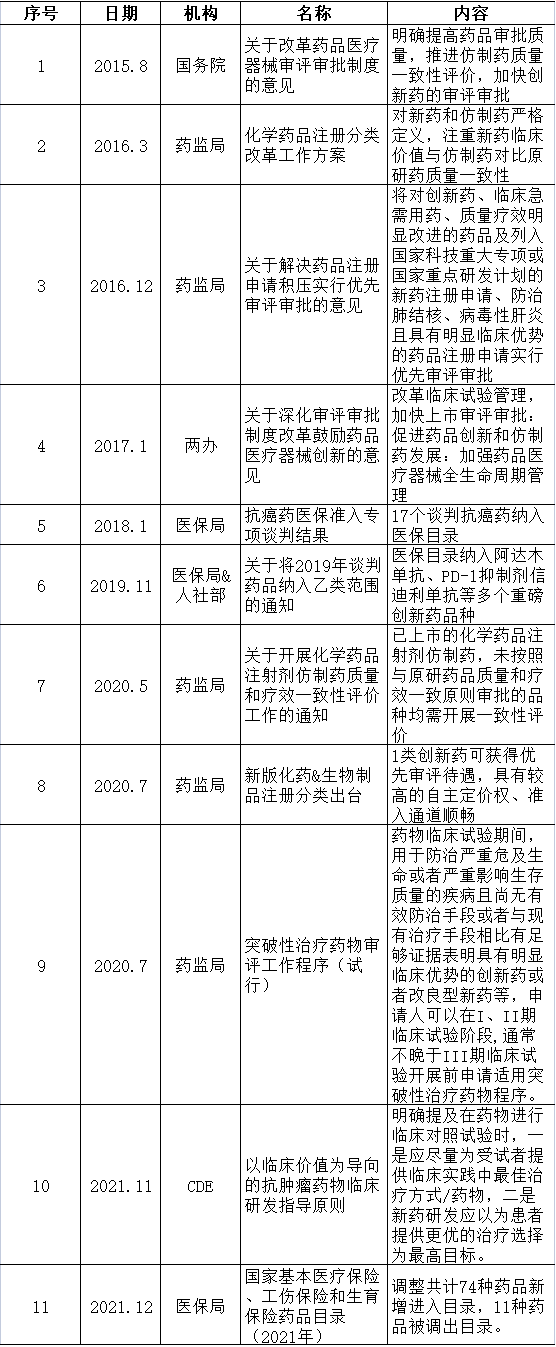
政策暖风驱动频吹,鼓励创新上升国家高度。目前,国内医药政策推动行业逐步加快由“仿制驱动”向“创新驱动”转变。自2015年8月以来,国家针对行业发展出台了多项鼓励政策:
1)审评审批加速:创新药纳入优先审评后直接缩短新药上市时间,加速新药获利时间,提高了药企新药研发积极性;
2)医保谈判准入:创新药上市后能通过医保谈判进入医保动态调整目录,加快新药放量速度,增加患者可及性;
3)配套政策:上市许可人制度、新化药注册分类等创新药配套政策,鼓励医药行业真正的创新。
表3 国家出台部分相关支持政策
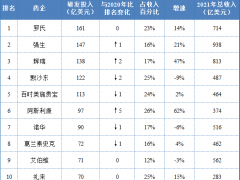
三、我国创新药行业市场规模分析
由于药品创新研发具有投入多、周期长及风险高等特点,过去,我国的医药行业一开始是以仿制药物为主,伴随着创新药审批、医保加强控费等政策出台以及经济快速发展带来创新药市场化提速,创新药在医药市场结构的比重逐渐加大,我国也正在经历“仿制药-难仿药-同类最佳-同类首创”的转变与突破。
据公开数据统计,2017年-2021年,中国创新药行业市场规模从1178亿美元增长到1455亿美元,年复合增长率为5.42%。中国创新药前景巨大,占医药市场的比重将明显提升。以美国、日本的市场为例,美国仿制药占全部药品处方量89.8%,销售额只有20.8%。日本仿制药占全部药品处方量79.9%,占药品销售额15%。而我国仿制药占全部药品处方95%,占全部药品销售额约40%。比对下来,中国的仿制药在药品处方量、销售额上还有将近20%的压缩空间,而这20%的份额很大程度将要让渡给创新药。

图1 2017-2021年中国创新药市场规模及预测(单位:亿美元)
在应用领域端,2018年以来,国家药品监督管理局药品审评中心(CDE)受理并批准上市的创新药数量逐年增长,适应症以抗肿瘤及免疫用药、神经系统用药、消化系统用药、抗感染药为主。
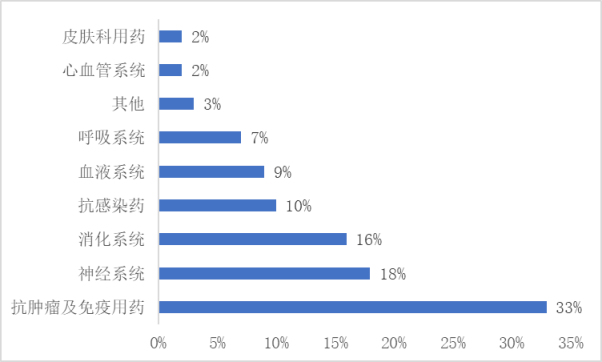
图2 2018-2021年获批上市创新药ATC分类分布
(数据来源:药智网、国家药品监督管理局药品审评中心)
四、我国创新药行业产业链
创新药行业产业链上游市场参与者,主要为创新药医药原材料及制药设备生产商;产业链中游环节主体主要包括化学创新药、中药创新药、生物创新药生产及销售企业;下游涉及创新药的销售终端,主要包括公立医疗机构、健康服务机构及线上线下的零售药店等;最后达到终端消费者。中上游企业具有强烈的创新需求和驱动力,成为整个产业价值创造的核心引擎。
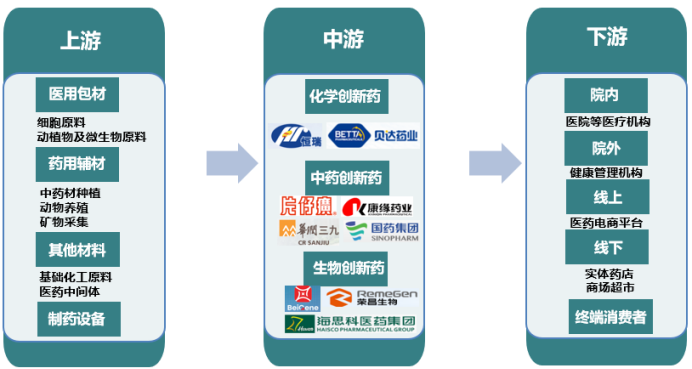
图3 我国创新药行业产业链图
五、我国创新药行业展望
临床价值是创新药的追求目标,创新药已成为我国医药产业技术升级,实现进口替代的必然需求。随着政策密集出台,带量采购常态化持续加速行业分化,倒逼企业向创新转型;医保目录已建立动态调整,也将促进企业端以价换量,加快药品入院进程,实现销售快速放量。政策大力推动以及市场创新研发更迭提速,我国医药创新将进入黄金发展期。
未来,同质化、伪创新产品将逐渐失去竞争力,创新药物的开发能力将成为药企的核心竞争力,稀缺技术平台、差异化治疗领域、创新给药方式等都将会给企业带来更好的竞争格局,伪创新药物市场空间将逐步被压缩殆尽。
同时,我国医药行业研发支出力度不断提升,跨国合作研究带动国内外技术差距不断缩小,更多创新药企选择将产品进行中美市场双认证上市,不但有助于走向国际,打开欧美市场,也标志着公司研发实力和临床申报能力达到较高认证水平,进而增强获取更高市场空间能力。
国际生物医药产业园Ⅱ期致力于打造成为国际领先,“专业、安全、高效”的国际生物医药产业标杆园区,及粤港澳大湾区一流的政、产、学、研协同创新的生物医药产业园。
编辑:胡其文
校对:卢小芳