作者:拾贝
4月7日,CDE官网显示,赛生医药注射用PEN-866钠临床申请获国家药监局受理。
PEN-866是赛生药业开发的一款小分子偶联药物(SMDC),目前正在美国开展针对实体瘤的II期篮式试验。
抗体偶联药物(ADC)无疑是时下最受关注的偶联药物代表,上市和临床药物的治疗突破和交易也备受关注;然而,ADC药物的缺陷也是显而易见,比如不能靶向胞内蛋白、复杂的生产工艺和监管挑战等。
与ADC不同,SMDC通过小分子实现靶向定位,并精准释放药物,也是偶联药物赛道中的潜力分支。SMDC和ADC药物的设计理念与作用机制相似,不过,SMDC仍有潜力穿透细胞膜靶向胞内蛋白。另一方面,就药物本身的外在体现而言,SMDC与传统化学药品并无太多不同。因此,成本控制、产能保障、监管合规、临床使用等诸多方面,都有长期积累的实战经验。
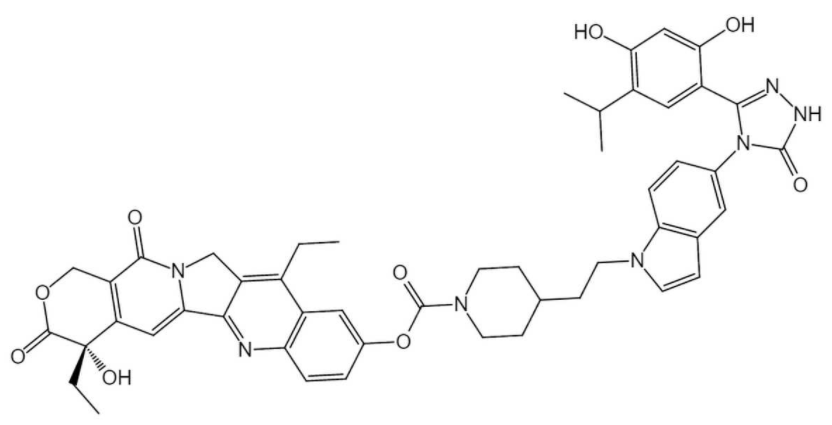
PEN-866结构式
重要的是,SMDC在临床表现上却具有和ADC相似的优势,特别是不良反应的控制。PEN-866通过可选择性的小分子与细胞内靶标热休克蛋白90 (HSP90) 结合,将毒素拓扑异构酶抑制剂伊立替康的活性代谢产物SN-38携带至肿瘤中积累并滞留,SN-38随着时间的推移被切割释放,避免了伊立替康(代谢出SN-38)全身暴露导致的不良反应。
临床数据显示,PEN-866在推荐剂量下(175 mg/m2),未观察到DLT(剂量限制性毒性),仅1位患者经历了无并发症的G3级一过性中性粒细胞减少症,相较于伊立替康高达53.8%的≥3级的中性粒细胞减少事件而言,安全性优势显著。
PEN-866最初由Tarveda开发,2020年3月,赛生药业与Tarveda达成合作协议,获得在大中华区(包括中国大陆、香港、澳门和台湾)共同开发和商业化PEN-866的独家授权。根据协议,赛生药业向Tarveda支付了400万美元的预付款,并有权在未来对Tarveda进行高达500万美元的股权投资,以及总计7500万美元的开发、批准和商业销售里程碑付款。
据悉,目前国内布局小分子偶联药物的企业包括同宜医药(CBP-1008、CBP-1018)、中国医学科学院基础医学研究所(DTX-P7)、赛生药业(PEN-866、T-2143)、台湾浩鼎生技(OBI-3424)。
注:原文有删减






