
来源:国家药监局官网
磷酸特地唑胺为利奈唑胺的衍生药物,是一款二代恶唑烷酮类抗生素,最初由韩国Dong-A制药研发,后由Merck和Bayer进行商业化开发,最早于2014年6月获得FDA批准上市,2015年6月在欧盟获批上市。
为应对滥用抗生素引起的新耐药性问题,美国于2012年7月通过了《鼓励开发抗生素法案》,符合标准的抗生素药物(经过QIDP认证)将获得额外五年的专利保护期,此外还加快了对抗菌药物的审批,磷酸特地唑胺是距离达巴万星上市仅仅一个月后批准的第二个用于治疗成人急性皮肤和皮肤组织(ABSSSI)感染的抗菌新药。
在国内,拜耳的磷酸特地唑胺片剂及注射剂于2019年3月获批进口,目前有10家国内企业以新注册分类提交注射用磷酸特地唑胺上市申请,其中扬子江的产品首家申报并成功拿下首仿;2家企业以新注册分类提交磷酸特地唑胺片上市申请,目前还在审评审批中。
磷酸特地唑胺新分类报产情况
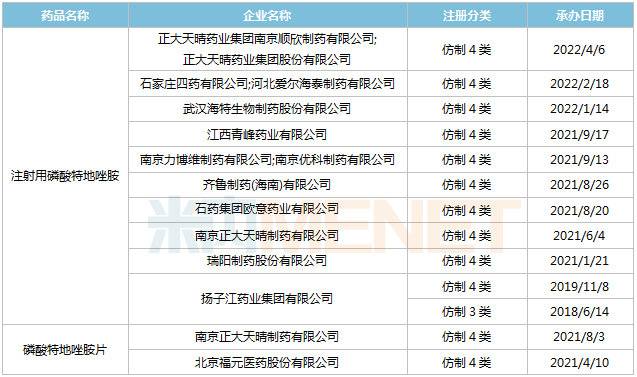
来源:米内网MED2.0中国药品审评数据库
左乙拉西坦是一种吡咯烷酮衍生物,可用于成人及4岁以上儿童癫痫患者部分性发作的加用治疗。目前国内已上市左乙拉西坦主要剂型包括注射剂、片剂、口服溶液剂等。
米内网数据显示,左乙拉西坦片在2020年中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院(简称中国公立医疗机构)及中国城市实体药店终端合计销售规模超过10亿元。
目前有十多家国内企业布局左乙拉西坦片一致性评价(含补充申请及新分类申报),其中扬子江、圣华曦、普洛康裕、京新药业、华海药业、信立泰、华润赛科、东北制药沈阳第一制药、四环制药9家企业的产品已通过或视同通过一致性评价。
来源:米内网数据库、上市公司公告






